PEG-N3与炔基的生物正交和点击化学

生物正交化学简介
? pH值:反应必须在生理环境的温度和pH值下发生;
? 精准:反应必须具有选择性并且高效得到目标产品,且须不受水或内源性亲核试剂、亲电试剂、还原剂或复杂生物环境中氧化剂的影响;
? 快速:即便在低浓度下,反应也必须是快速的,并且须生成稳定的反应产物;
? 特异性:反应应涉及生物系统中非天然存在的官能团。
生物正交反应的优点和缺点
生物正交反应 | 优点 | 缺点 |
Staudinger 连接反应 | 叠氮化物和膦化物具有生物相容性,生成的产物是以稳定的酰胺键连接的。 | 反应速度慢,磷化氢容易被氧化。 |
CuAAC(叠氮+炔基) | 反应迅速,在20 μM Cu(I)的催化下k值可达~10-100(M-1S-1);具有良好的区域选择性。 | 尽管有些配体如THPTA比较稳定,但是铜催化剂的铜毒性仍需考虑在内。 |
SPAAC(叠氮+DBCO) | 无需铜催化,k值约~1-60 (M-1S-1)。 | 1. 反应慢于CuAAC,大块的环状砌块难以融入生物分子; 2.?所需溶剂:10%-40%的乙醇溶液或DMSO(至多60%)/PBS缓冲液; 3.?pH < 5.5时反应速度会变慢,因为在此pH下DBCO的稳定性会降低; 4.?巯基、叠氮化钠都会与DBCO发生反应。 |
IEDDA (TCO + Tz) | 反应非常迅速,k值约~1-106?(M-1S-1) | TCO在含水环境中稳定性差。 |
表1:各类生物正交反应的优缺点小结表
经典的点击化学反应会用到铜作为催化剂,一般是一价铜催化1,3-偶极环加成炔和叠氮化物形成1,2,3-三唑[1,2]。一价铜的来源包括碘化铜、溴化铜、
铜屑或硫酸铜与还原剂发生反应生成的产物[3]。然而,一价铜具有热力学不稳定性,容易被氧化成无活性的二价铜,通常需要铜催化剂与合适的螯合配体共同制备。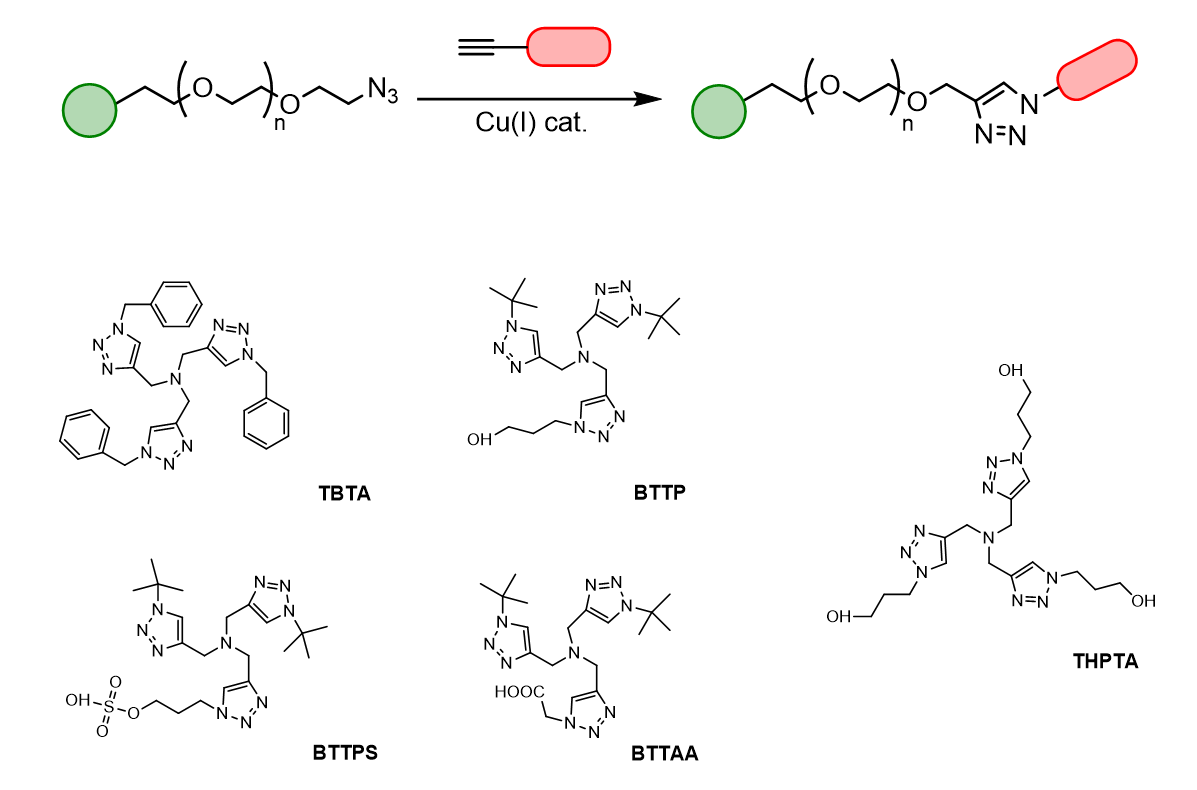
TBTA覆盖了在点击化学领域的大量实际应用,除了含水环境下的共轭反应。而水溶性的THPTA点击配体则可以适用于水相反应,进一步简化点击化学步骤,为点击化学反应提供具生物相容性的THPTA配体来结合Cu(I),阻断Cu(I)的生物利用度,改善其潜在的毒性作用,保持催化效率
[4]。同时THPTA配体可以有效地被用于高效标记活细胞,并维持细胞活性[5]。我们发现THPTA在水相反应中是一种高效的点击化学配体,它的标记反应在室温下往往只需要15-30分钟即可完成。在冷冻条件下储存,配体CuSO4
复合物在至少一个月后仍能保持原有的活性。
实操案例
1.?配制以下原液:
? 200 mM THPTA配体的水溶液
? 100 mM硫酸铜水溶液
? 炔基标记的水相寡聚物
? 100 mM抗坏血酸钠水溶液
? 10 mM在DMSO/叔丁醇或水中的含叠氮化合物
2. 在反应前将硫酸铜和THPTA配体以1:2的当量比混合静置几分钟,这样的溶液在冷冻后可以稳定储存数周;
3. 向寡聚糖/DNA溶液中添加过量4~50倍当量的叠氮化物(如PEG-N3等);
4. 添加25当量的THPTA/CuSO4;
6. 在室温下静置反应30~60分钟;
7. 在乙醇中沉淀纯化寡聚物。
细胞裂解物的标记
1.?配制以下原液:
? 100 mM THPTA配体的水溶液或缓冲溶液
? 20 mM硫酸铜水溶液
? 300 mM抗坏血酸钠水溶液
? 2.5 mM在水或DMSO中的炔基或叠氮标记试剂
2.?对每个叠氮化物或炔基修饰的蛋白质裂解物样品,添加以下物质至1.5 mL的离心管中,然后简单涡旋混合:
? 50 μL存放于蛋白质萃取缓冲液中的蛋白质裂解产物(1-5 mg/mL)
? 90 μL PBS缓冲液
? 20 μL在水中或DMSO中2.5 mM相应叠氮化物(或含炔基化合物)的检测试剂
3. 加入10 μL的100 mM THPTA溶液并简单涡旋混合;
4. 加入10 μL的20 mM硫酸铜溶液并简单涡旋混合;
5. 加入10 μL的300 mM 抗坏血酸钠溶液来引发点击化学反应并简单涡旋混合;?
6. 保护反应避光,并在室温下反应30分钟;
7. 现在在裂解物中的蛋白质已通过点击化学反应被标记了,可以进行下一步的处理和分析了。
铜催化的炔基-叠氮化物点击化学标记活细胞
叠氮聚糖在HeLa和CHO细胞表面的标记及共聚焦显微镜成像
参考文献
2. Analysis and Optimization of Copper-Catalyzed Azide–Alkyne Cycloaddition for Bioconjugation; V. Hong, S. I. Presolski, C. Ma, M. G. Finn,?Angew. Chem. Int. Ed.?2009,?48, 9879.?https://onlinelibrary.wiley.com/doi/10.1002/ange.200905087
3. Stabilization of Virus-like Particles with Poly(2-oxazoline)s; F. Manzenrieder, R. Luxenhofer, M. Retzlaff, R. Jordan, M. G. Finn,?Angew. Chem. Int. Ed.?2011,?50, 2601.?https://onlinelibrary.wiley.com/doi/10.1002/ange.201006134
4. Synthesis of Cyclic Peptide Disulfide–PHPMA Conjugates via Sequential Active Ester Aminolysis and CuAAC Coupling; K. A. Günay, H. Klok,?Polym. Chem.?2016,?7, 970.?https://pubs.rsc.org/en/content/articlelanding/2016/py/c5py01817j
5. Cellular Consequences of Copper Complexes used to Catalyze Bioorthogonal Click Reactions; D. C. Kennedy, C. S. McKay, M. C. B. Legault, D. C. Danielson, J. A. Blake, A. F. Pegoraro, A. Stolow, Z. Mester, J. P. Pezacki,?J. Am. Chem. Soc.?2011,?133, 17993.?https://pubs.acs.org/doi/10.1021/ja2083027
 首页
首页 400-620-6333
400-620-6333



 危险品化学品经营许可证(带存储)
危险品化学品经营许可证(带存储)