羟醛缩合反应
什么是羟醛缩合反应?
醛醇缩合反应是由Charles Wurtz提出的一种有机反应,他于1872年首次从乙醛中制备出β-羟基醛[1]。在醛醇缩合反应中,烯酸盐离子与羰基化合物在酸/碱催化剂的存在下反应生成β-羟基醛或β-羟基酮,随后脱水得到共轭的烯酮。是一种有效的碳-碳成键反应。醛醇缩合反应的基本步骤是:
1. 醛醇(醛+醇)反应-醛(或酮)烯酸酯与醛(或酮)的另一分子在NaOH或KOH存在下反应,形成β-羟基醛(或酮)。
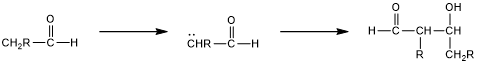
2. 脱水/消除反应——从β-羟基醛(或酮)中除去水分子,形成α,β-不饱和醛或α,β-不饱和酮。
请参阅安全数据表,以了解有关危害和安全处理措施的信息。
应用场景
醛醇缩合反应可用于以下合成:
· 脂肪酸的酶促合成[2]
· 埃博霉素B的高效全合成[3]
· ?(E)-6-(2,2,3-三甲基-环戊-3-烯基)-己-4-烯-3-酮的制备[4]:
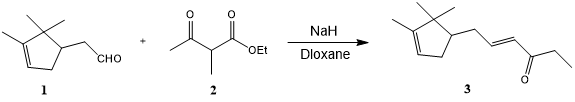
将2-甲基乙酰乙酸乙酯(2)(727 mg, 4.53 mmol)添加至NaH?(184 mg, 4.60 mmol)存于二氧六环(25 mL)中之搅拌溶液中。然后添加莰烯醛(1)(707 mg, 3.72 mmol)并将混合物回流15 h。然后添加2N HCl?(15 mL)并用Et2O (3×15 mL)萃取混合物。用2N HCl (2×15 mL)、饱和Na2CO3?(2×15 mL)和盐水(3×15 mL)洗涤合并的有机层。经无水Na2SO4干燥有机相并且在减压下蒸发溶剂,得到残余物(900 mg),在减压下通过蒸馏纯化残余物,得到标题化合物3?(505 mg, 2.63 mmol, 58%)。
· 聚戊二醛高聚物的合成[5]
· (±)-麻黄碱的立体选择性合成[6]
· 大环内酯类和离子载体抗生素(天然产物)的合成[7]
· 两种结构独特的四环喹诺酮类化合物——双螺旋胺A和B的全合成[8]

该路线分为三步,通过5-溴-4-甲氧基羰基甲氧基喹啉与乙烯基硼酸酯的Suzuki交叉偶联,然后进行α-酮羟基化和分子内醛醇缩合和内酯化的双环化,从而获得吡喹喹啉丁烯内酯环。随后通过对侧链的操作,引入胍片段,完成了双螺旋胺B的合成,而双螺旋胺A的同系物是由后期中间体脱羧作用得到的。
· 采用水溶性杯芳烃作为反相转移催化剂,对活化的甲基和亚甲基化合物进行了醛缩合和迈克尔加成反应[9]
· 采用含铯离子催化剂,在SBA-15介孔分子载体上进行乙酸甲酯与甲醛的缩合反应[10]
该催化剂在缩合反应中表现出较高的催化活性。XRD表征表明,低于5 wt%负载的硝酸铯在SBA-15支架上高度分散。FT-IR和XPS结果证实催化剂表面形成Si-O-Cs。NH3-TPD和CO2-TPD结果表明,弱Lewis酸碱对负载在表面,这些弱酸碱活性位点可能有利于醛醇缩合反应。5Cs/SBA-15催化剂表现出最高的乙酸甲酯转化率(48.4%)和95.0%的丙烯酸甲酯选择性。失活催化剂经煅烧完全再生。催化剂再生9次,总操作时间超过60 h,乙酸甲酯的初始转化率和对丙烯酸甲酯的选择性均未发生变化。催化剂具有较高的催化活性,主要是由于载体表面的Si-O-Cs基团具有较强的弱酸碱性质。
· 环己酮与对硝基苯甲醛在水中的有机催化不对称醛醇反应[11]
· 一锅法铜催化醚化/醛醇缩合级联反应制备二苯并西平内酰胺[12]
· 通过烷基化、区域选择性碘化、醛醇缩合、Suzuki偶联和[1,3]-sigma重排等方法合成一系列二戊烯化和二癸基化查尔酮类似物[13]
· 在KOH存在的甲醇溶剂中,苊醌与苯乙酮进行迈克尔加成和醛醇缩合,可形成多米诺骨牌序列,从而进一步形成了不同的2:2加合物[14]
· 缩醛反应通常会利用酸性或碱性催化剂进行,因此,MCM-41的改性是通过两个酸性基团(3-丙基磺基、3-丙基羧基)和一个碱性基团(3-(1,2-二乙基氨基)丙基)后接枝法实现的,采用的是经硫酸和硝酸处理的MCM-41[15]。用BET、元素分析和UV-Vis光谱对所制备的功能化材料进行了表征。结果表明,最佳反应条件为反应混合物温度100℃,反应物4-异丙基苯甲醛:丙醛的摩尔比为1:2,催化剂的用量和种类为50 wt%的MCM SO3H(与4-异丙基苯甲醛的用量相比),丙醛的加入时间为90分钟,反应的适宜溶剂为甲苯。在最佳反应条件下,甲醛的收率为45%。将所得结果与H2SO4均相催化的效果进行了比较,其收率为15%。
参考文献
1. Nielsen?AT,?Houlihan?WJ.?The Aldol Condensation. 1-438.?https://doi.org/10.1002/0471264180.or016.01
2. Brady?RO.?1958.?The Enzymatic Synthesis of Fatty Acids by Aldol Condensation.?Proceedings of the National Academy of Sciences.?44(10):993-998.?https://doi.org/10.1073/pnas.44.10.993
3. Balog?A,?Haris?C,?Savin?K,?Zhang?X,?Chou?T,?Danishefsky?S.?1998.?Angew. Chem. Int. Ed..?372675.
4. Badía?C,?Castro?J,?Linares Palomino?P,?Salido?S,?Altarejos?J,?Nogueras?M,?Sánchez?A.?(E)-6-(2,2,3-Trimethyl-cyclopent-3-enyl)-hex-4-en-3 one.?Molbank.?2004(1): M388.?https://doi.org/10.3390/m388
5. Tashima?T,?Imai?M,?Kuroda?Y,?Yagi?S,?Nakagawa?T.?1991.?Structure of a new oligomer of glutaraldehyde produced by aldol condensation reaction.?J. Org. Chem..?56(2):694-697.?https://doi.org/10.1021/jo00002a038
6. Heathcock?CH,?Buse?CT,?Kleschick?WA,?Pirrung?MC,?Sohn?JE,?Lampe?J.?1980.?Acyclic stereoselection. 7. Stereoselective synthesis of 2-alkyl-3-hydroxy carbonyl compounds by aldol condensation.?J. Org. Chem..?45(6):1066-1081.?https://doi.org/10.1021/jo01294a030
7. Masamune?S,?Choy?W,?Kerdesky Francis A. J.,?Imperiali?B.?1981.?Stereoselective aldol condensation. Use of chiral boron enolates.?J. Am. Chem. Soc..?103(6):1566-1568.?https://doi.org/10.1021/ja00396a050
8. Jolibois?AER,?Lewis?W,?Moody?CJ.?2014.?Total Synthesis of (±)-Distomadines A and B.?Org. Lett..?16(4):1064-1067.?https://doi.org/10.1021/ol403598k
9. Shimizu?S,?Shirakawa?S,?Suzuki?T,?Sasaki?Y.?2001.?Water-soluble calixarenes as new inverse phase-transfer catalysts. Their application to aldol-type condensation and Michael addition reactions in water.?Tetrahedron.?57(29):6169-6173.?https://doi.org/10.1016/s0040-4020(01)00572-5
10. Yan?J,?Zhang?C,?Ning?C,?Tang?Y,?Zhang?Y,?Chen?L,?Gao?S,?Wang?Z,?Zhang?W.?2015.?Vapor phase condensation of methyl acetate with formaldehyde to preparing methyl acrylate over cesium supported SBA-15 catalyst.?Journal of Industrial and Engineering Chemistry.?25344-351.?https://doi.org/10.1016/j.jiec.2014.11.014
11. Mase?N,?Nakai?Y,?Ohara?N,?Yoda?H,?Takabe?K,?Tanaka?F,?Barbas?CF.?2006.?Organocatalytic Direct Asymmetric Aldol Reactions in Water.?J. Am. Chem. Soc..?128(3):734-735.?https://doi.org/10.1021/ja0573312
12. Lim?HS,?Choi?YL,?Heo?J.?2013.?Synthesis of Dibenzoxepine Lactams via a Cu-Catalyzed One-Pot Etherification/Aldol Condensation Cascade Reaction: Application toward the Total Synthesis of Aristoyagonine.?Org. Lett..?15(18):4718-4721.?https://doi.org/10.1021/ol402036t
13. Wang?H,?Zhang?L,?Liu?J,?Yang?Z,?Zhao?H,?Yang?Y,?Shen?D,?Lu?K,?Fan?Z,?Yao?Q,?et al.?2015.?Synthesis and anti-cancer activity evaluation of novel prenylated and geranylated chalcone natural products and their analogs.?European Journal of Medicinal Chemistry.?92439-448.?https://doi.org/10.1016/j.ejmech.2015.01.007
14. Domino reaction sequences leading to the formation of 2:2 adducts between acenaphthenequinone and acetophenone.?2014(6):127.?https://doi.org/10.3998/ark.5550190.p008.834
15. Vrbková?E,?Vyskocilová?E,?Cerveny?L.?2015.?Functionalized MCM-41 as a catalyst for the aldol condensation of 4-isopropylbenzaldehyde and propanal.?Reac Kinet Mech Cat.?114(2):675-684.?https://doi.org/10.1007/s11144-014-0811-2
 首页
首页 400-620-6333
400-620-6333



 危险品化学品经营许可证(带存储)
危险品化学品经营许可证(带存储)